Lupus und Irinotecan
Eigentlich bin ich Chirurg und inzwischen spezialisiert auf die Thoraxchirurgie. Als akademisch tätiger Chirurg war ich viele Jahre Leiter einer Arbeitsgruppe, die sich mit Krebsforschung beschäftigte. Mit Lupus erythematodes oder anderen Autoimmunkrankheiten hatte ich wie man so sagt „Nichts am Hut“ und ehrlich gesagt wusste ich darüber auch nur das Wenige, woran ich mich noch aus dem Studium erinnern konnte. Bis zu jenem Experiment vor ungefähr sieben Jahren, was als ganz normales Krebsforschungsexperiment begonnen hatte. Der Befund war so ungewöhnlich, dass ich ein halbes Jahr darüber nachdachte und dann anschließend mit meiner Arbeitsgruppe die Entscheidung traf, dieser Sache nachzugehen.
Unser Zufallsbefund führte zu der Hypothese, dass Irinotecan in der Lage ist, bestimmte fatal verlaufende Überempfindlichkeitsreaktionen zu verhindern. Wir begannen mit Anaphylaxie und scheiterten, wir machten weiter mit Autoimmundiabetes und scheiterten abermals. Zu diesem Zeitpunkt war ich schon fast entschlossen, das Ganze als Hirngespinst abzutun und die Experimente in dieser Richtung abzubrechen, als plötzlich unsere Lupusmäuse erstaunliche Dinge zeigten.
Die Mäuse, die wir für unsere Experimente einsetzten, sind eine Kreuzung aus zwei natürlich vorkommenden Mausstämmen, den New Zealand Black and New Zealand White, woraus sich auch ihr Name NZB/W ableitet. NZB/W Mäuse entwickeln im Laufe ihres Lebens spontan eine Lupuskrankheit, die mit Glomerulonephritis einhergeht und auch sonst viele Ähnlichkeiten zu menschlichem SLE hat.[1] Verwendet wird dieses Tiermodel zur Erforschung von SLE seit mehr als 6 Jahrzehnten. Wobei die überwiegende Mehrzahl der bisher publizierten Experimente einen Behandlungsbeginn vor Ausbruch der Krankheit beinhaltete und es bisher nur ganz wenige Forschungsgruppen schafften, NZB/W mit bereits bestehender Lupusnephritis (das heisst mit schwergradiger Eiweissausscheidung – Proteinurie -) erfolgreich zu behandeln. Interessanterweise erbrachte auch die heutige Standardmedikation der Lupusnephritis keine überzeugenden Daten in dieser Richtung.[2] [3] [4]
Unter Verwendung von Irinotecan konnten wir dann zeigen, dass NZB/W mit weit fortgeschrittener Erkrankung positiv auf die Behandlung reagierten, indem die Proteinurie vermindert und die Lebensdauer fast verdoppelt wurde.[5] Ein negativer Aspekt an unserer damaligen Entdeckung war aber, dass die damals gebrauchten Dosierungen von Irinotecan denen zur Chemotherapie im Menschen verwendeten gleich waren. Somit war es fraglich, ob Irinotecan als eine neue Therapieoption für überwiegend junge Frauen in Frage kommen würde. Wir begannen daraufhin eine Serie von Experimenten, die eine Verminderung der Irinotecan-Dosis zum Ziel hatten. Abbildung 1 zeigt ein solches Experiment, welches den Effekt einer Dosis zeigt, die ca. 8-mal tiefer als die zur Chemotherapie im Menschen verwendete Dosierung ist. Schlussendlich zeigten unsere Experimente, dass eine Dosis, die 50-mal tiefer als die zur Chemotherapie verwendete ist, immer noch fortgeschrittene Lupusnephritis verbessert und die Lebensdauer deutlich verlängert.[6]
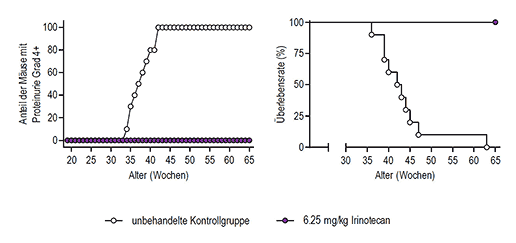 Abbildung 1: Verhinderung von Lupusnephritis und Verlängerung der Lebensdauer durch niedrig dosiertes Irinotecan in NZB/W Mäusen. Das Entstehen der Lupusnephritis wurde anhand der Eiweißausscheidung im Urin (Proteinurie) gemessen, wobei Grad 4+ dem höchstmöglichen Krankheitsgrad entspricht. (veröffentlicht in Arthritis Rheumatol. 2014 Aug;66(8):2259-69)
Abbildung 1: Verhinderung von Lupusnephritis und Verlängerung der Lebensdauer durch niedrig dosiertes Irinotecan in NZB/W Mäusen. Das Entstehen der Lupusnephritis wurde anhand der Eiweißausscheidung im Urin (Proteinurie) gemessen, wobei Grad 4+ dem höchstmöglichen Krankheitsgrad entspricht. (veröffentlicht in Arthritis Rheumatol. 2014 Aug;66(8):2259-69)Die Vermutung, dass eine derart tiefe Dosis nichts mehr mit einer Chemotherapie (und auch deren Nebenwirkungen) zu tun hat, wurde durch weitere Experimente bestätigt. Diese Untersuchungen hatten das Ziel, den zellbiologischen Mechanismus aufzuklären, wie Irinotecan Lupusnephritis unterdrückt. Bis zum heutigen Zeitpunkt erbrachten wir in diesem Zusammenhang folgende Resultate:
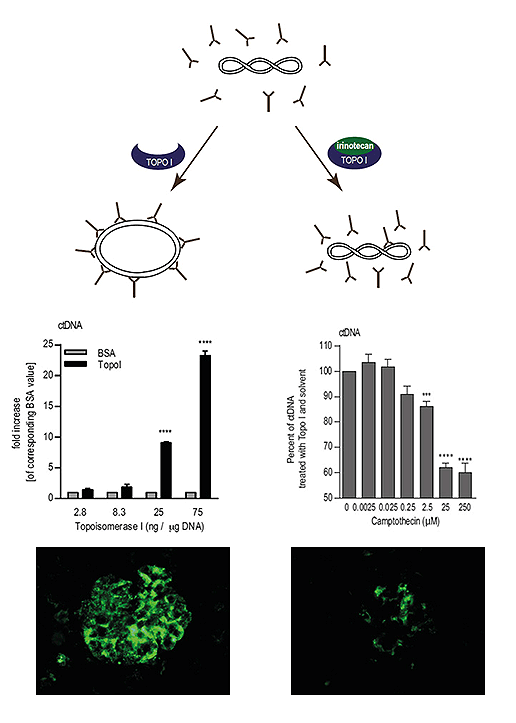 Abbildung 2: Schematische Darstellung wie der Grad der DNA-Entspannung die Entstehung von Lupusnephritis bedingen könnte und wie dieser Prozess möglicherweise durch den Topoisomerase I Inhibitor Irinotecan positiv beeinflusst wird (veröffentlicht in J Immunol. 2010 Feb 15;184(4):2175-82 und Arthritis Rheumatol. 2014 Aug; 66(8): 2259-69)
Abbildung 2: Schematische Darstellung wie der Grad der DNA-Entspannung die Entstehung von Lupusnephritis bedingen könnte und wie dieser Prozess möglicherweise durch den Topoisomerase I Inhibitor Irinotecan positiv beeinflusst wird (veröffentlicht in J Immunol. 2010 Feb 15;184(4):2175-82 und Arthritis Rheumatol. 2014 Aug; 66(8): 2259-69)- Irinotecan bewirkt im Gegensatz zu bisher verwendeten Lupusmedikamenten nur eine milde und vorübergehende Unterdrückung des Immunsystems.[5], [6]
- Irinotecan bewirkt in der Lupusniere eine Unterdrückung des programmierten Zelltodes (Apoptose).[5] Im Gegensatz dazu bewirkt Irinotecan als Chemotherapeutikum bei Krebserkrankungen eine Induktion von Apoptose.
- Irinotecan beeinflusst den Entspanntheitsgrad von DNA im Zusammenhang mit Topoisomerase I, und dieser Prozess hat wiederum Auswirkungen auf die Bindung von Lupus-spezifischen Auto-Antikörpern, die gegen doppelsträngige DNA gerichtet sind: Lange Zeit dachten wir, dass die es Erzeugung von DNA-Einzelstrangbrüchen durch die kombinierte Behandlung mit Topoisomerase I und Irinotecan ist, die den positiven Effekt auf den Krankheitsverlauf von Lupusnephritis erzeugt.[7] Bis wir zufällig entdeckten, dass Topoisomerase I allein das Bindungsverhalten von Auto-Antikörpern gegen doppelsträngige DNA erhöht (Abbildung 2, Mitte links). Dieser Effekt wird durch die Zugabe von Irinotecan gestoppt bzw. umkehrbar gemacht (Abbildung 2, Mitte rechts).[6] Ob dieser bisher nur im Reagenzglas gezeigt Effekt auch für die Verminderung schädlicher Antikörperkomplexe in den Nieren von Irinotecan behandelten NZB/W verantwortlich ist (Abbildung 2 unten),[5] ist Gegenstand zukünftiger Forschungsprojekte.
- ↑ Hahn, B.H. Lessons in lupus: the mighty mouse. Lupus 10, 589-593 (2001).
- ↑ Casey, T.P. Immunosuppression by cyclophosphamide in NZB X NZW mice with lupus nephritis. Blood 32, 436-444 (1968).
- ↑ Casey, T.P. Azathioprine administration to NZB X NZW hybrid mice with lupus nephritis: beneficial effect complicated by development of malignant lymphomas. N Z Med J 79, 290-295 (1973).
- ↑ Steinberg, A.D., Gelfand, M.C., Hardin, J.A. & Lowenthal, D.T. Therapeutic studies in NZB/W mice. III. Relationship between renal status and efficacy of immunosuppressive drug therapy. Arthritis Rheum 18, 9-14 (1975).
- ↑ Frese-Schaper, M., Zbaeren, J., Gugger, M., Monestier, M. & Frese, S. Reversal of established lupus nephritis and prolonged survival of New Zealand black x New Zealand white mice treated with the topoisomerase I inhibitor irinotecan. J Immunol 184, 2175-2182 (2010).
- ↑ Frese-Schaper, M., et al. Low-dose irinotecan improves advanced lupus nephritis in mice potentially by changing DNA relaxation and anti-double-stranded DNA binding. Arthritis Rheumatol 66, 2259-2269 (2014).
- ↑ Frese, S. & Diamond, B. Structural modification of DNA-a therapeutic option in SLE? Nat Rev Rheumatol 7, 733-738 (2011).

